最全備案——這些間充質干細胞進展你應該了解!
最新數據,截至2020年11月,中國醫藥生物技術協會又公布了13個通過備案的干細胞臨床研究項目(我國干細胞臨床研究備案項目已經近100例,詳情見附表),其中近80%使用的是間充質干細胞。

圖片來源于網絡,侵刪
間充質干細胞由于其自我更新與多向分化潛能,近年來成為了醫學重點攻關的對象。這一方向的研究,奠定了間充質干細胞在難治性疾病治療中重要地位,現如今,間充質干細胞針對各種適應癥的臨床研究越來越多。
研究進展
國際進展
根據ClinicalTrials的最新數據,以“stem cells”為關鍵詞搜索,全球目前有8259例臨床研究,其中已完成3303項,主要完成疾病種類包括自身免疫性疾病、卵巢早衰、新冠肺炎、性功能障礙、心腦血管疾病、糖尿病、膝骨關節炎等。
圖片來源:ClinicalTrials
國內進展
據國家藥監局藥品審評中心(CDE)官網信息,2018 年 6 月至今,國內已經有 9 款干細胞新藥 IND 獲得臨床默示許可,分別是胎盤、臍帶、異體 / 自體脂肪來源的間充質干細胞,適應癥分別為腦卒中、急性腸炎、類風濕關節炎、糖尿病足潰瘍、膝骨關節炎和類風濕關節炎。
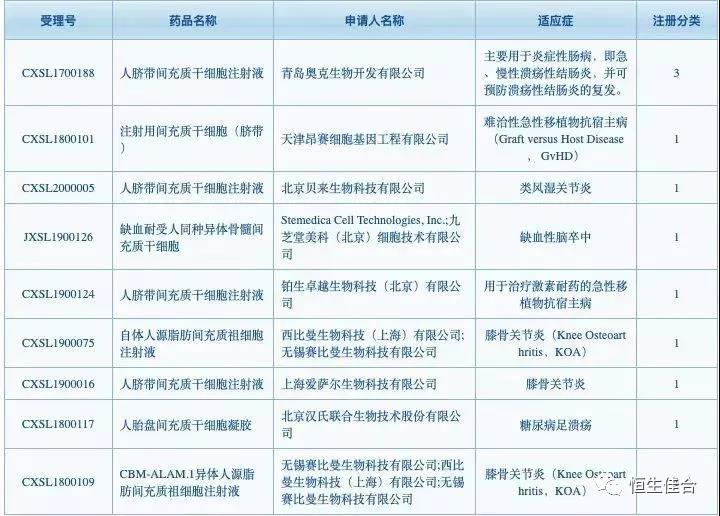
圖片來源:國家藥監局藥品審評中心
政策盤點
【2020年8月 CDE】
國家藥品監督管理局藥品審評中心組織起草了《人源性干細胞及其衍生細胞治療產品臨床試驗技術指導原則(征求意見稿)》,以期為藥品研發注冊申請人及開展藥物臨床試驗的研究者提供更具針對性的建議和指南。
【2020年4月 國家藥監局】
國家藥監局關于發布《藥品生產質量管理規范(2010年修訂)》生物制品附錄修訂稿的公告。

此前,在2018年國家知識產權局發布《知識產權重點支持產業目錄(2018年本)》,就將干細胞與再生醫學、免疫治療、細胞治療等明確列為國家重點發展和亟需知識產權支持的重點產業之一。


迄今為止“干細胞及轉化研究”已獲得了五次中央財政經費支持。
2016年,25個擬立項項目(包含青年科學家項目)獲得了約4.88億元的經費支持;
2017年,43個擬立項項目又再獲9.4億元的經費支持。
2018年度發表于中國生物技術發展中心的“干細胞及轉化研究”重點專項擬立項項目共計30個,總經費5.85億元,項目周期均為2018-2022年。

另據2018年8月21日科技部公布的《“ 干細胞及轉化研究” 試點專項2019 年度項目申報指南( 征求意見稿)》顯示,2019年,中央財政將再撥款4個億給予支持!

今年2020年3月科技部發布了《科技部關于發布國家重點研發計劃“干細胞及轉化研究”等重點專項2020年度項目申報指南的通知》。2020年,國撥總經費 2.40億元。
研究進展
“用最科學的方法,使自己的身體變得更強大。”干細胞療法不論針對患者、科研人員,還是用來改變當前醫療行業現狀而言無疑都是很好的選擇。從發展歷程來看,干細胞對于難治性疾病治療、再生醫學領域,美容保健領域等給我們創造了很多奇跡,為患者和更多的家庭帶來了新的希望;從發展趨勢來看,未來的5~10年里干細胞行業將會有更大的進展。
附:干細胞臨床研究備案項目匯總
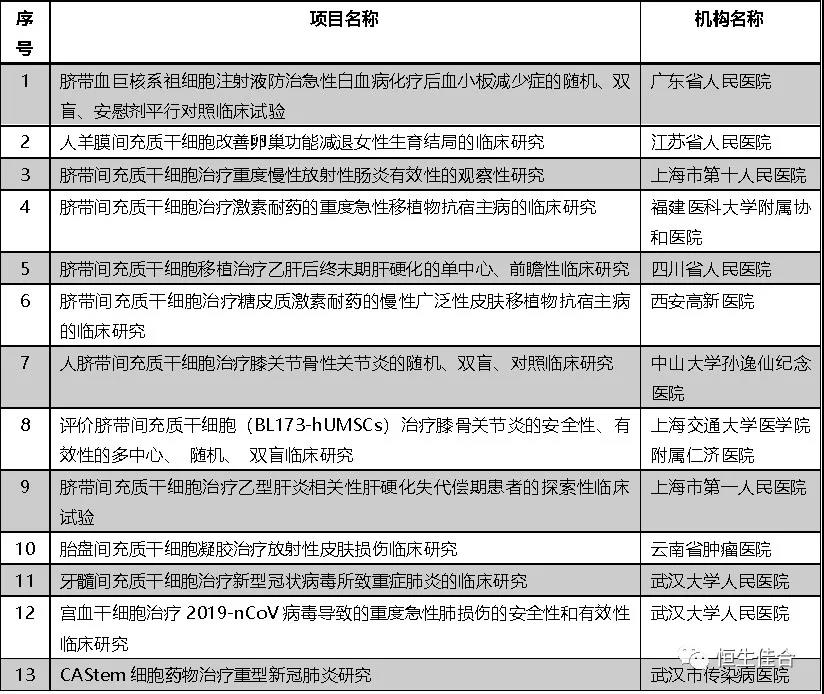
2020年11月,廣東省人民醫院等十二家醫療機構的13個干細胞臨床研究項目按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定完成備案。
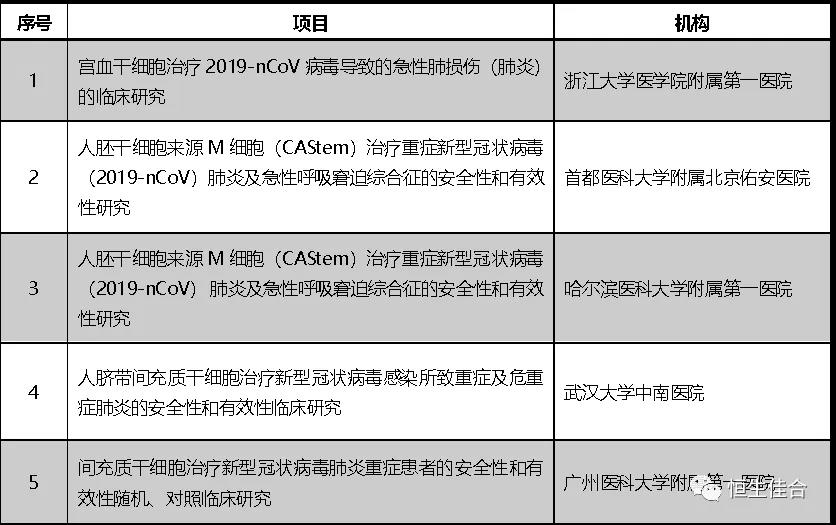
截止2020年3月19日浙江大學醫學院附屬第一醫院等五家醫療機構四個項目先后在國家兩委局完成備案。
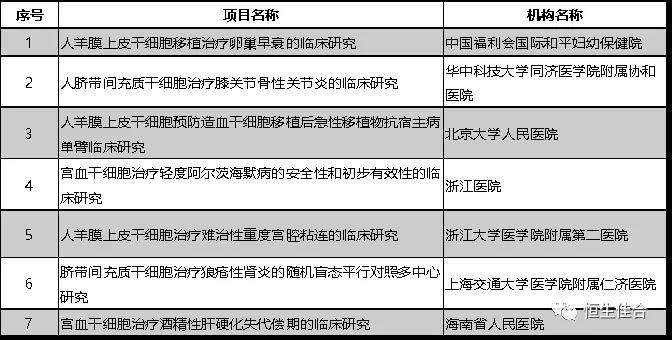
2019年12月,按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定,以及《關于做好2019年干細胞臨床研究監督管理工作的通知》(國衛辦科教函〔2019〕169號)文件精神,7個干細胞臨床研究項目符合備案要求完成備案。
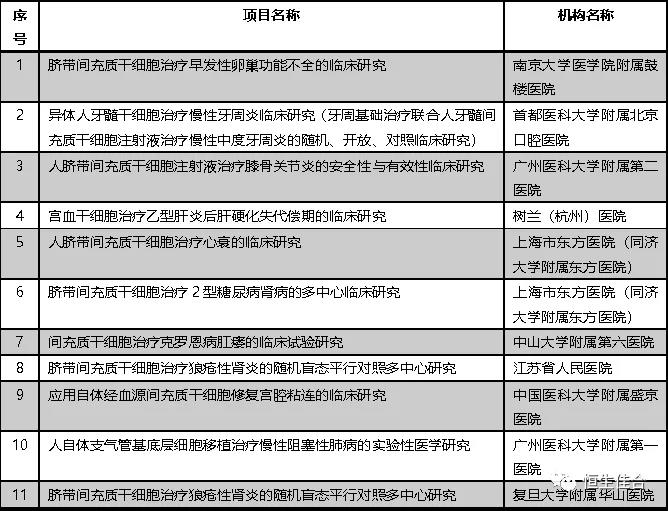
2019年9月,按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定,以及《關于做好2019年干細胞臨床研究監督管理工作的通知》(國衛辦科教函〔2019〕169號)文件精神,又有11個干細胞臨床研究項目完成備案。
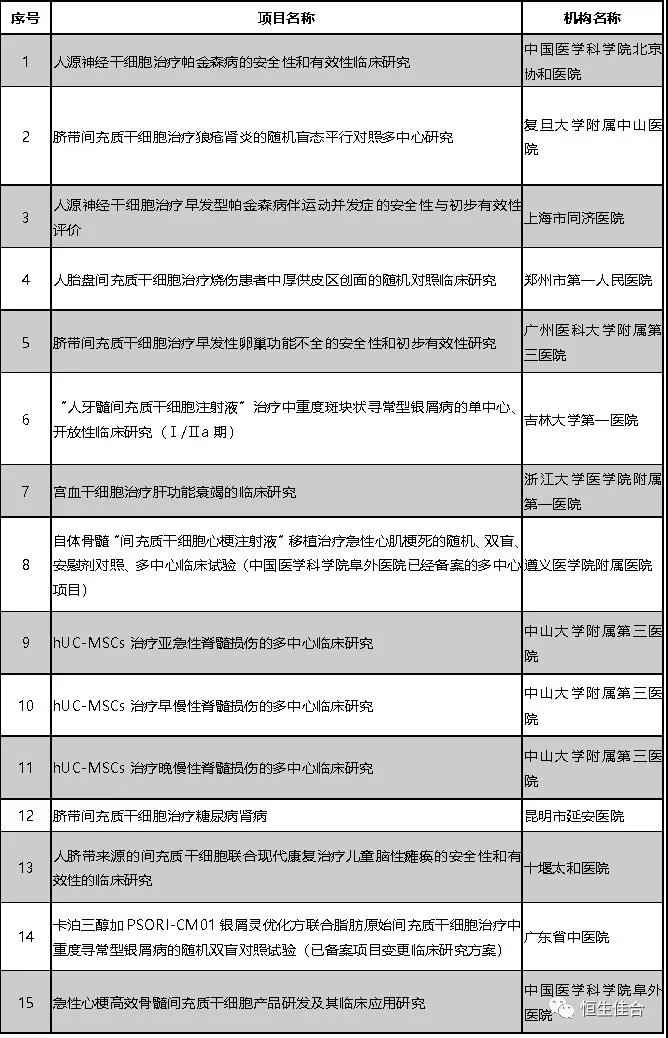
2019年6月,按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定,以及《關于做好2019年干細胞臨床研究監督管理工作的通知》(國衛辦科教函〔2019〕169號)文件精神,又有15個干細胞臨床研究項目完成備案。
2019年3月,按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定,上海交通大學醫學院附屬仁濟醫院、青島大學附屬醫院的2個干細胞臨床研究項目完成備案。蘭州大學第一醫院申報的干細胞臨床研究機構和項目同時完成備案。

2019年1月,安徽省立醫院等8個干細胞臨床研究項目按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定完成備案。
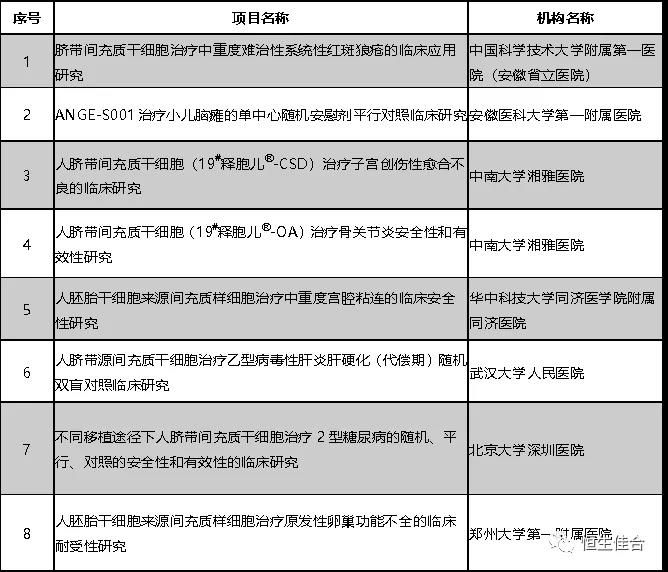
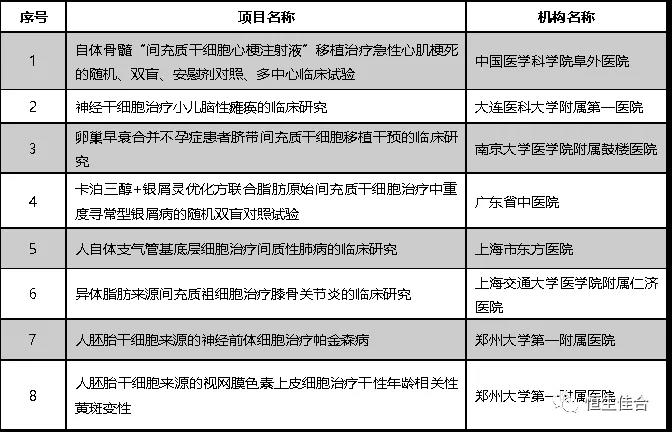
截至2018年9月,繼第二批十家機構的12個干細胞臨床研究項目備案之后,又7個干細胞臨床研究項目按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定完成備案。
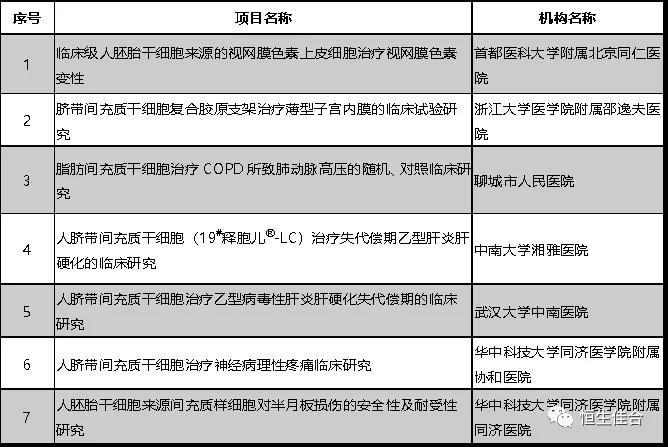
截至2018年5月,繼第一批七家機構的8個干細胞臨床研究項目備案之后,又12個干細胞臨床研究項目按照《干細胞臨床研究管理辦法(試行)》(國衛科教發〔2015〕48號)的規定完成備案。
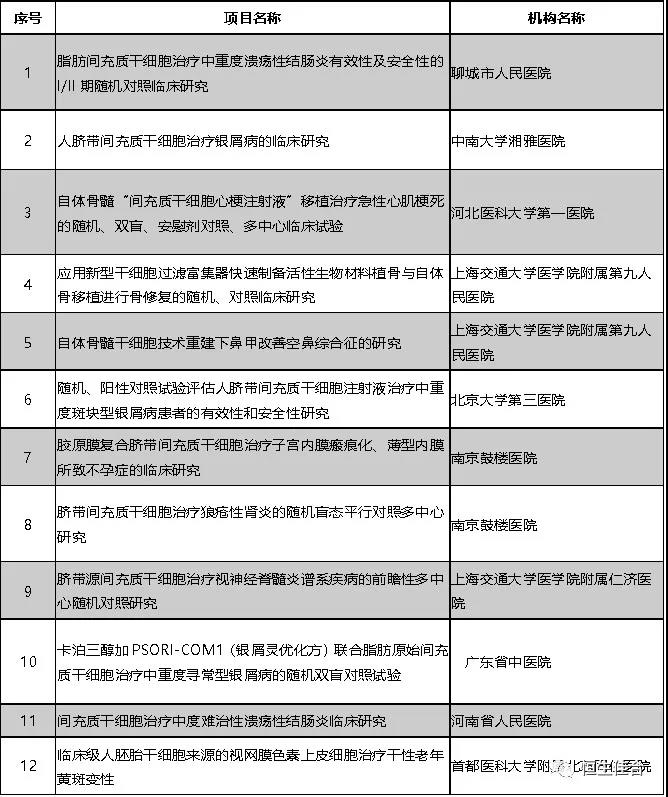
按照《干細胞臨床研究管理辦法(試行)》(國衛科教發【2015】48號)的規定,8個干細胞臨床研究項目完成備案,并已按規定在醫學研究登記備案信息系統登記,研究的摘要信息可以在系統查詢。